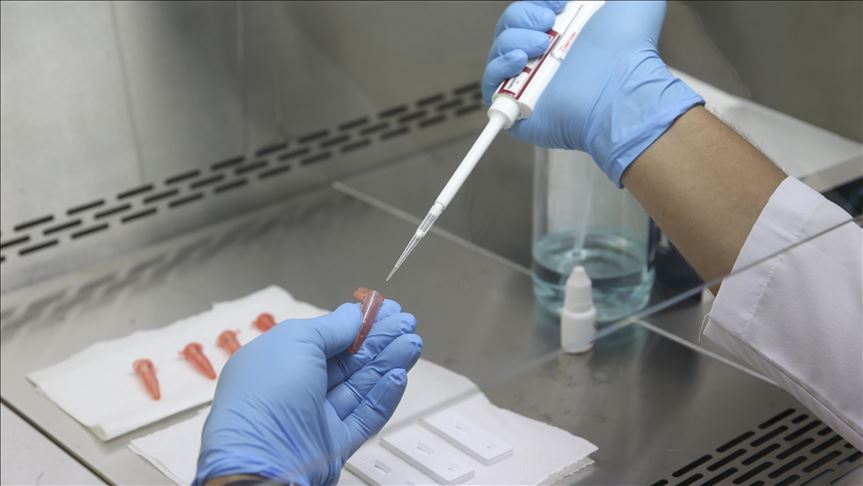
Los directivos de nueve compañías dicen que desarrollarán y probarán vacunas de acuerdo con «altos estándares éticos y principios científicos sólidos».
Nueve corporaciones biofarmacéuticas globales se comprometieron este martes a realizar un desarrollo seguro, pruebas, presentaciones regulatorias globales y aprobaciones de posibles vacunas para el coronavirus.
Las empresas incluyen a GlaxoSmithKline, AstraZeneca, BioNTech, Sanofi, Moderna, Novavax, Pfizer, Johnson & Johnson y Merck (esta última, conocida como MSD fuera de EEUU y Canadá).
Los jefes de las compañías dijeron en una declaración conjunta que están comprometidos «a mantener la integridad del proceso científico mientras trabajan hacia posibles presentaciones y aprobaciones regulatorias globales de las primeras vacunas contra la COVID-19», y dijeron que desarrollarían y probarían posibles vacunas de acuerdo con «altos estándares éticos y principios científicos sólidos».
«Creemos que este compromiso ayudará a garantizar la confianza del público en el riguroso proceso científico y normativo mediante el cual se evalúan las vacunas y, en última instancia, se pueden aprobar», agregaron en una declaración conjunta.
Si bien las empresas han desarrollado colectivamente más de 70 vacunas contra enfermedades a nivel mundial, la carrera por una vacuna contra la COVID-19 está a todo su ritmo.
Además de las naciones occidentales, Rusia aprobó una vacuna en agosto a pesar de que los expertos occidentales expresaron su preocupación por la falta de pruebas adecuadas.
En China, Sinovac Biotech anunció el domingo que el 90% de sus empleados y sus familias han tomado una vacuna experimental.
En Estados Unidos, el país más afectado por el virus, el jefe de la Administración de Alimentos y Medicamentos (FDA), Stephen Hahn, dijo el 30 de agosto que podría considerar la posibilidad de acelerar una vacuna antes de la conclusión de los ensayos de fase III.
Los comentarios de Hahn se produjeron una semana después de que la FDA aprobara el uso de emergencia de plasma para tratar a pacientes con COVID-19 en hospitales, a pesar de las preocupaciones de los funcionarios de salud.
Hahn dijo que no sería una «decisión política» apresurar una vacuna, pero el presidente de Estados Unidos, Donald Trump, acusó a la FDA de intentar afectarlo en las inminentes elecciones presidenciales de 2020, al actuar lentamente en el tratamiento del virus y el proceso de desarrollo de la vacuna.
La administración Trump ha implementado la Operación Warp Speed con la esperanza de obtener y administrar millones de dosis de una vacuna para fines de 2020.
En julio, acordó pagar a Pfizer y BioNTech USD 1.950 millones por 100 millones de dosis de su vacuna si resulta «segura y eficaz», mientras que anunció un acuerdo de USD 1.600 millones con Novavax para fabricar y distribuir 100 millones de dosis para enero de 2021.
Estados Unidos tiene más de 6.3 millones de casos y más de 189.000 muertes por COVID-19, según datos de la Universidad Johns Hopkins.
Fuente: Agencia de noticias Anadolu.